Bleiakkumulator Chemische Erklärung
Einleitung
In diesem Artikel soll sich mit den Chemischen Abläufen innerhalb eines Bleiakkus beschäftigt werden. Hierzu wird zunächst die Reaktion direkt nach dem Zusammenbau des Akkus erklärt und danach das Verhalten bei Laden und auch beim Entladen des Bleiakkus.
⇨ Bleiakku allgemein erklärt
Voller Akku

Leerer Akku

Bleiakku Aufbau
Um einen Bleiakku aufzubauen benötigen wir:
→ Ein Säurefestes Gehäuse
→ 2 Bleiplatten
→ Schwefelsäure (Elektrolyt)
→ Und Separatoren
In das Säurefeste Gehäuse werden die 2 Bleiplatten (Pb), wie hier gezeigt verbaut. Eine dient als positiv gepolte Elektrode, eine dient als negativ gepolte Elektrode.
Hinzu kommt der Separator.
Zudem wird in den Behälter 37%iger Schwefelsäure – Schwefelsäure welche mit Wasser verdünnt ist – hineingegossen. Man spricht dabei von Schwefelsäure in dissoziierter Form (xxxx).
Bleiakku Entladevorgang
Bevor der Akku Entladen wird, ist dieser voll geladen. Dabei besteht die negative Elektrode vollständig aus Blei(Pb) und die positive Elektrode aus Bleioxid (PbO2).
Das Elektrolyt ist …. und besteht aus Schwefeloxid Molekülen und Wasserstoffionen.
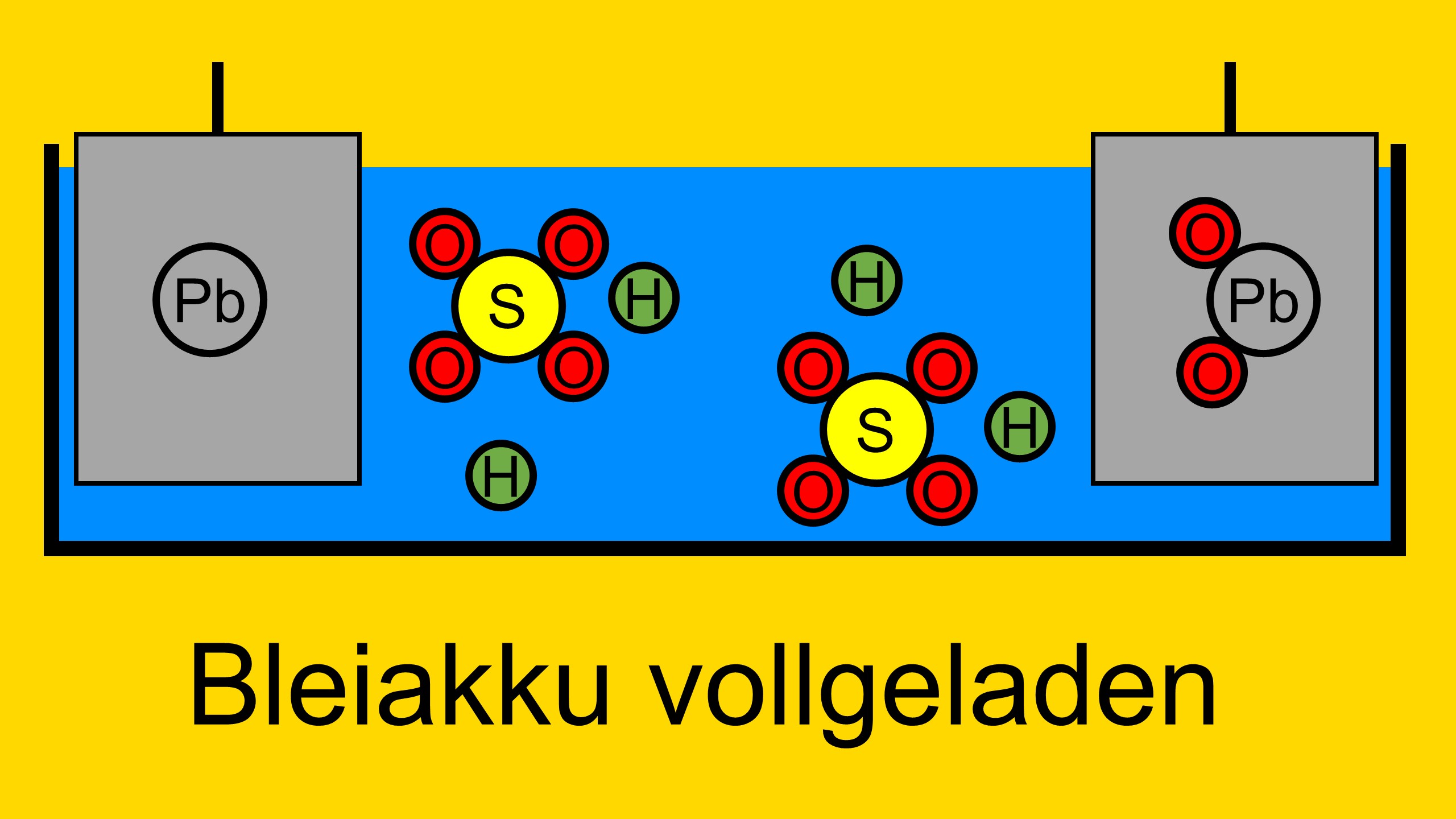
Bei Entladevorgang verbindet sich zunächst das Schwefeloxid (SO4) aus dem Elektrolyt mit dem Blei (Pb) der negativen Elektrode. Dabei werden Elektronen frei.

Wird nun ein Verbraucher angeschlossen, fließen die Elektronen zur positiven Elektrode. Dort trennen sie das Bleioxid (PbO2) auf. Es entsteht Blei (Pb) und Sauerstoff (O2).
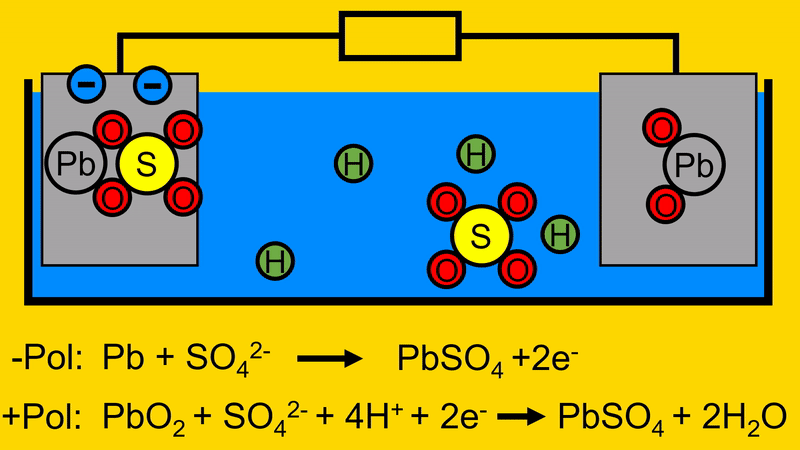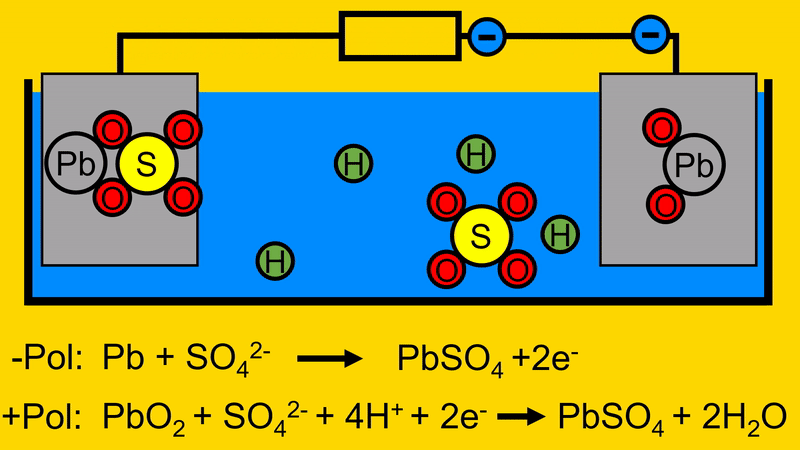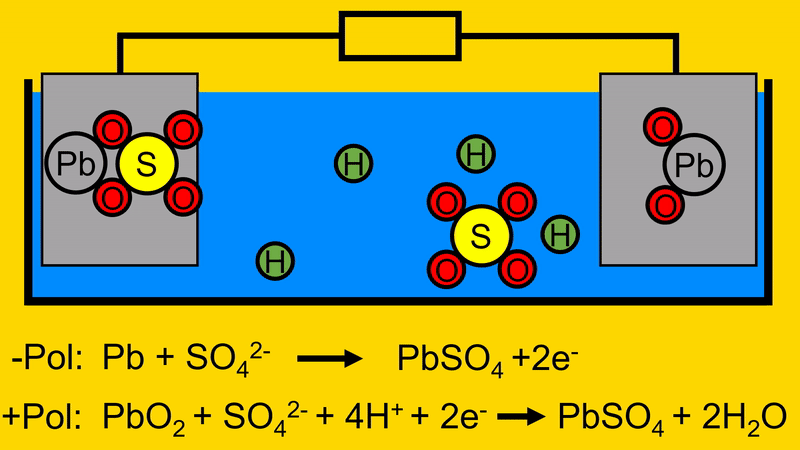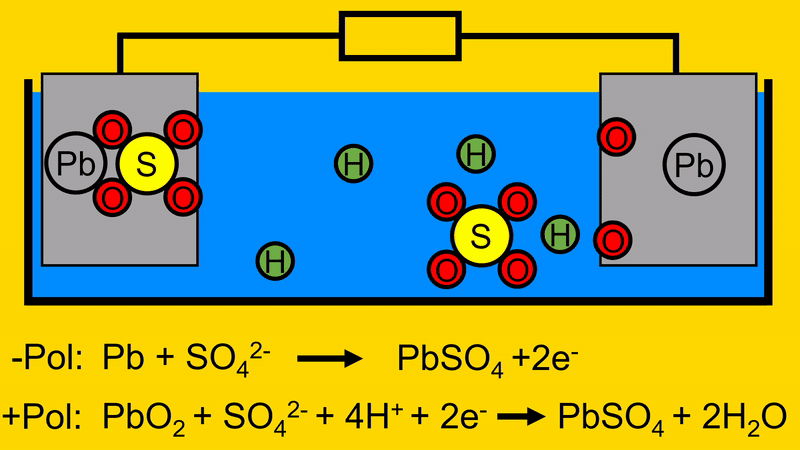
Der Sauerstoff (O2) verbindet sich mit dem Wasserstoff (H) aus dem Elektrolyt. Es bildet sich Wasser (H2O)
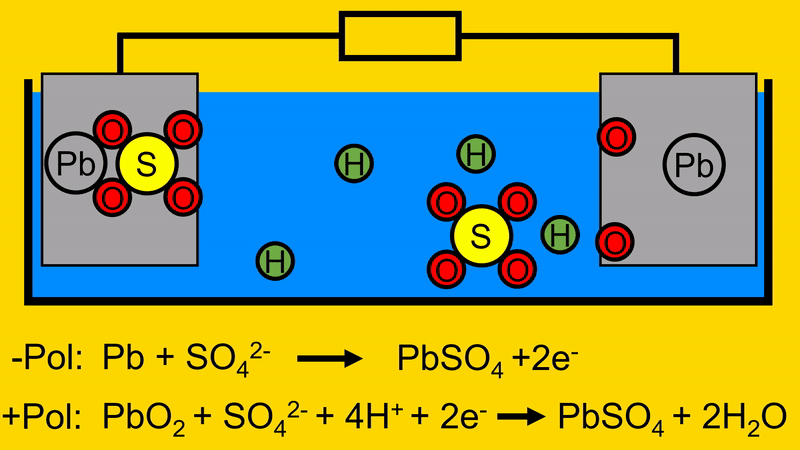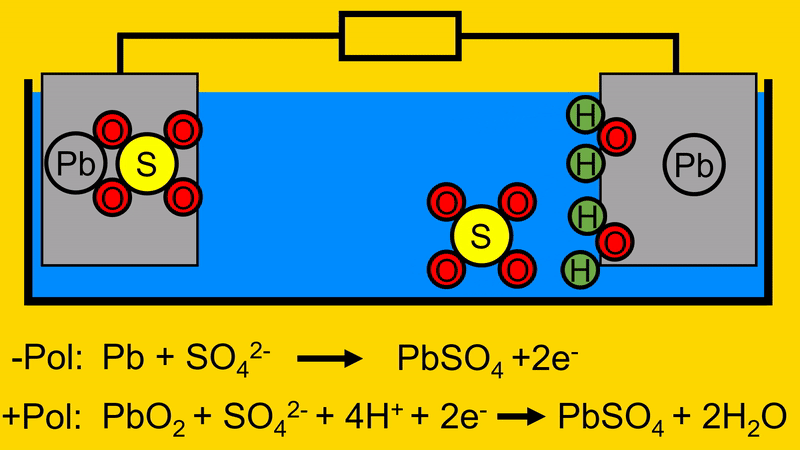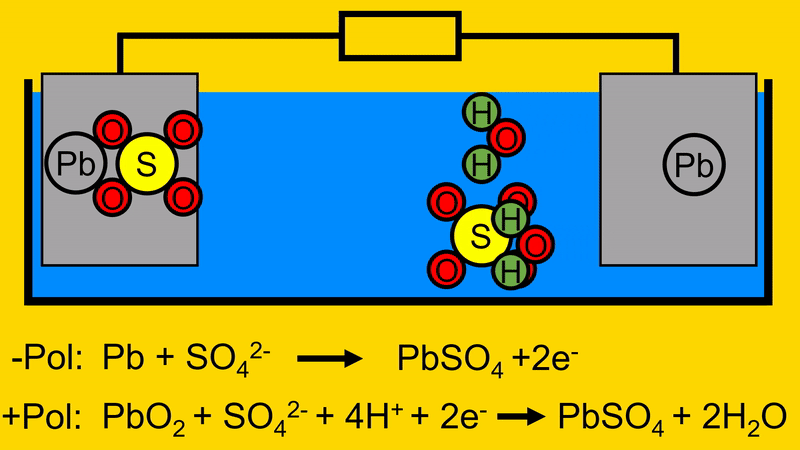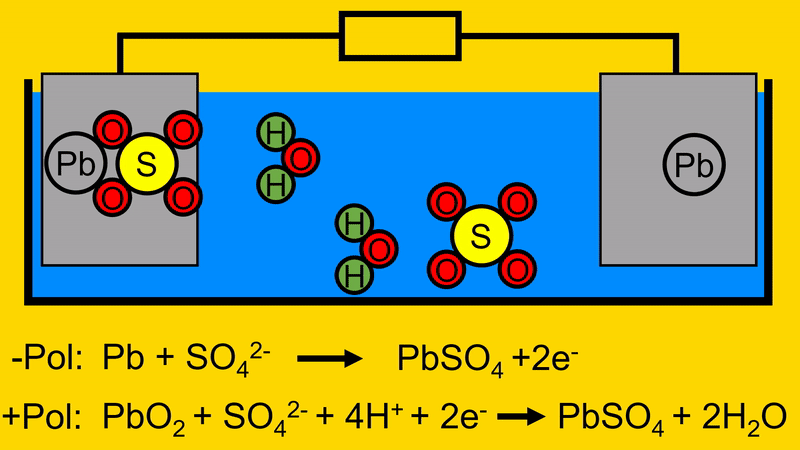
Das übrige Blei (Pb) in der positiven Elektrode verbindet sich, im Anschluss daran, mit dem Schwefeloxid (SO4).

Schritt für Schritt
→ Schritt 1:
Das So4 verbindet sich mit dem Blei (Pb) in der negativen Elektrode.
→ Schritt 2:
Dabei werden 2 Elektronen (2e) freigesetzt. Welche sich in der negativen Elektrode sammeln.
→ Schritt 3:
Wird nun ein Verbraucher angeschlossen, fließen die Elektronen zum +Pol.
→ Schritt 4:
Dort trennen die Elektronen beim PbO2 das Blei (Pb) vom Sauerstoff (O2).
→ Schritt 5:
Das nun freie O2 löst sich von der positiven Elektrode und verbindet sich mit dem H. So bildet sich H2O.
→ Schritt 6:
Nun verbindet sich das SO4 mit dem Blei (Pb) in der positiven Elektrode.
Zusammenfassung:
Bei der Entladung sinkt die Konzentration des Elektrolyts immer weiter ab. Das bedeutet das Elektrolyt wird immer wässriger.
Während dieses Vorgangs fließen Elektronen vom -Pol zum +Pol.
Bleiakku Ladevorgang
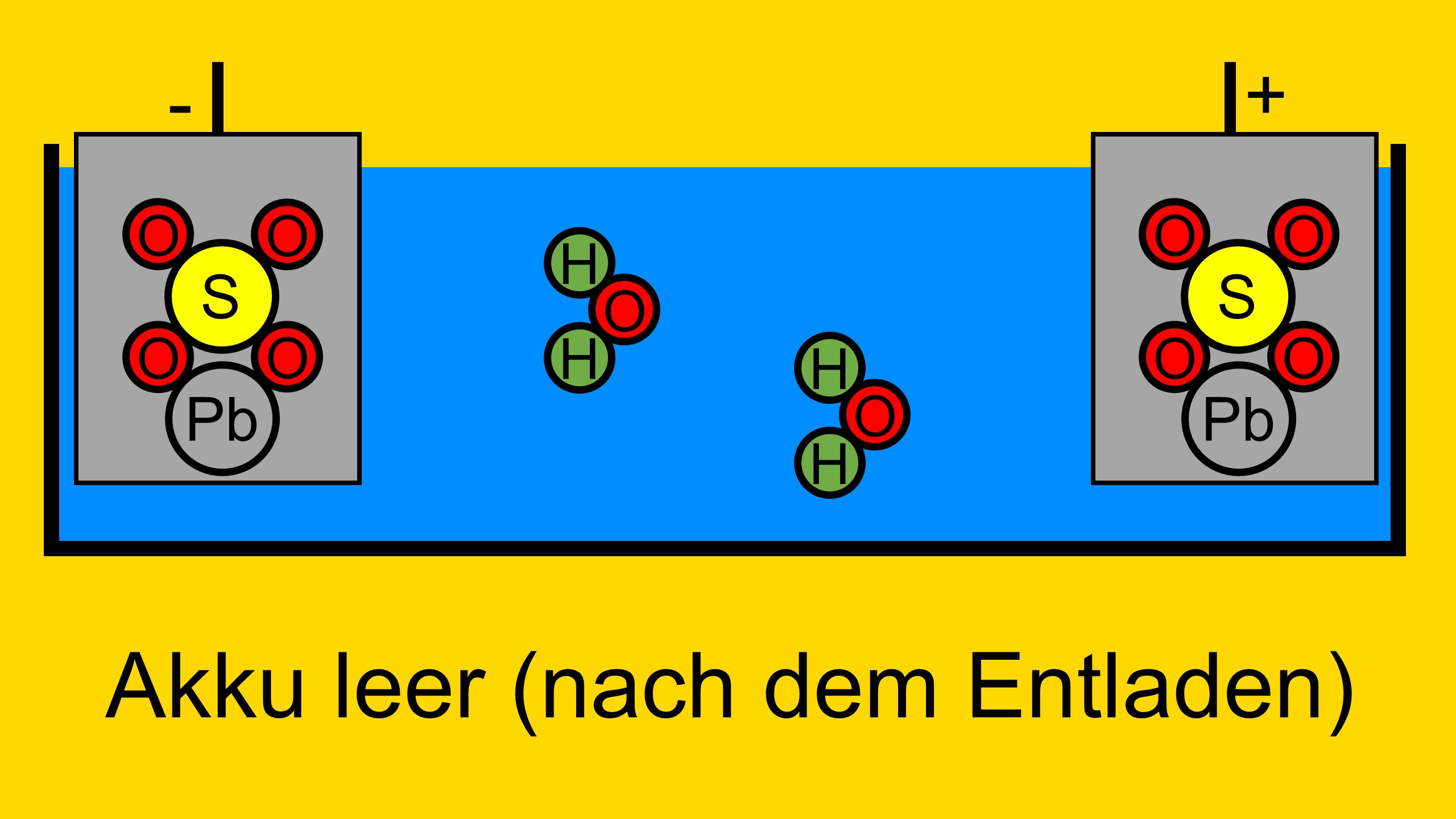
Bevor der Akku aufgeladen wird, ist dieser leer. Dabei besteht die negative und die positive Elektrode aus Blei-Schefeloxid (PbSO4).
Das Elektrolyt besteht aus Wasser (H2O).
Bei Ladevorgang wird eine Spannungsquelle (hier in Form einer Batterie) an die Elektroden angeschlossen. Dabei fließen Elektronen in die negative Elektrode. Hierdurch trennt sich das BleiSchwefeloxid auf. Das Blei bleibt auf der negativen Elektrode zurück. Das Schwefeloxid geht in das Elektrolyt.
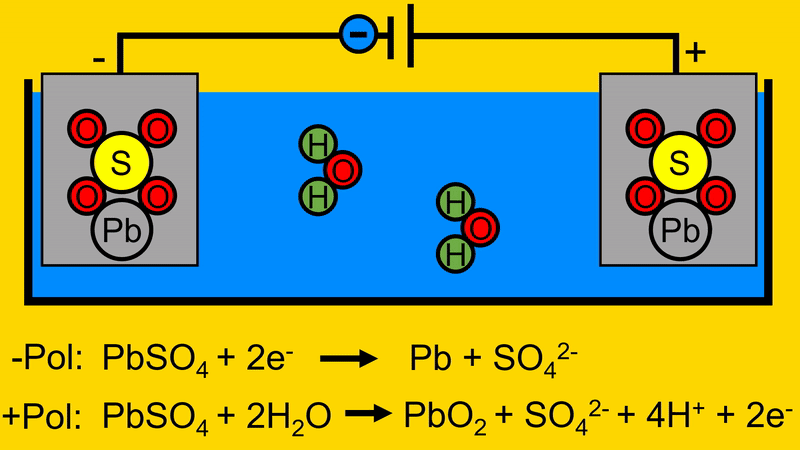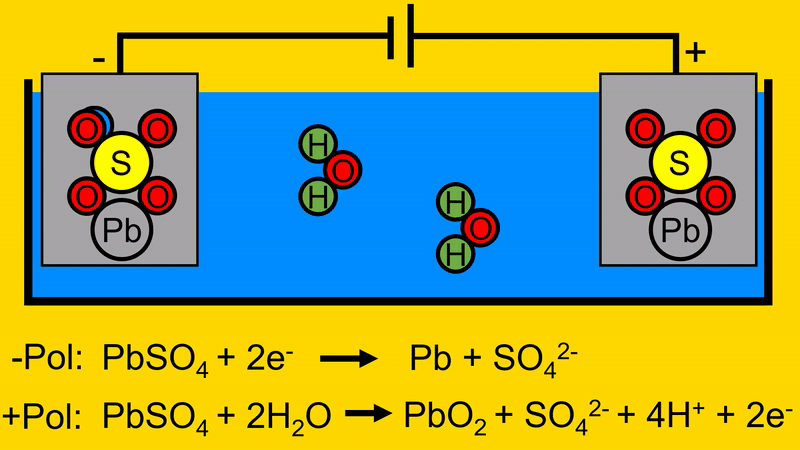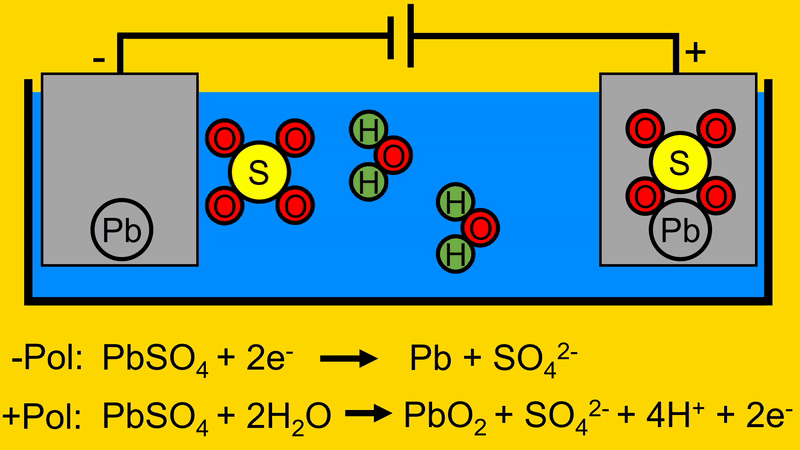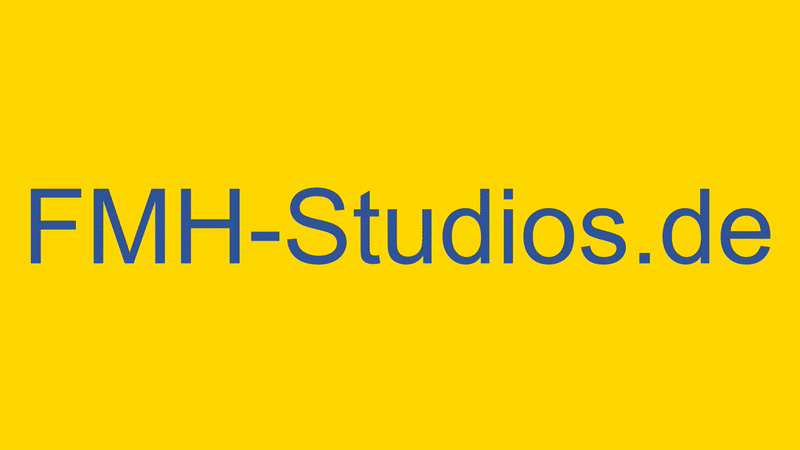
Der Sauerstoff aus dem Wasser verbindet sich mit dem Blei-Schwefeloxid auf der positiven Elektrode.
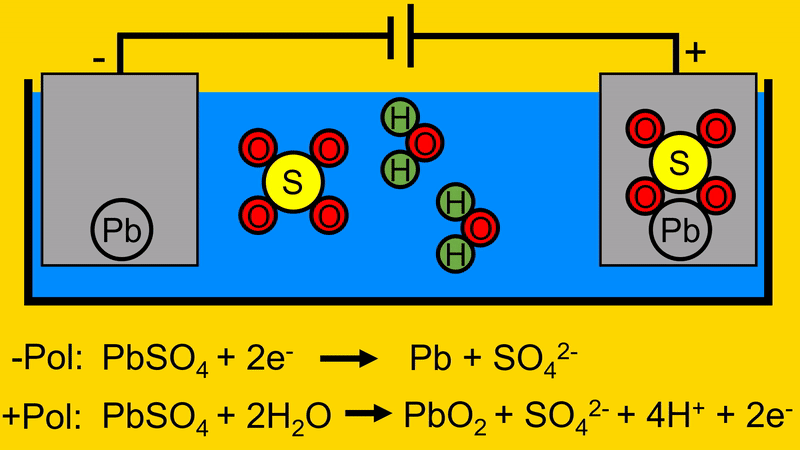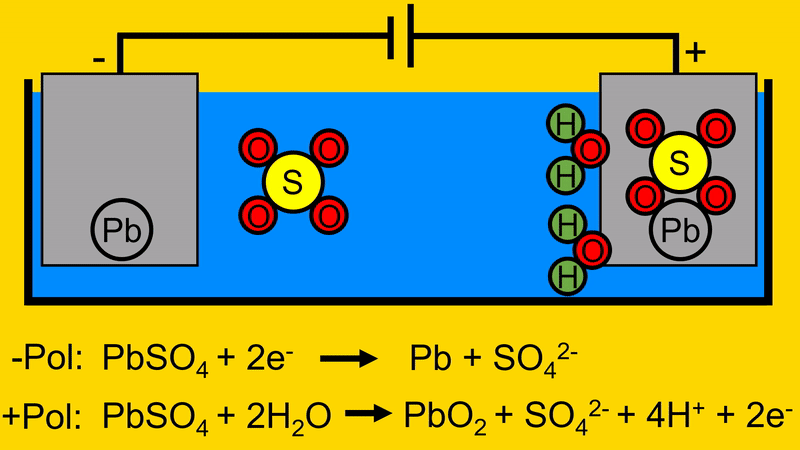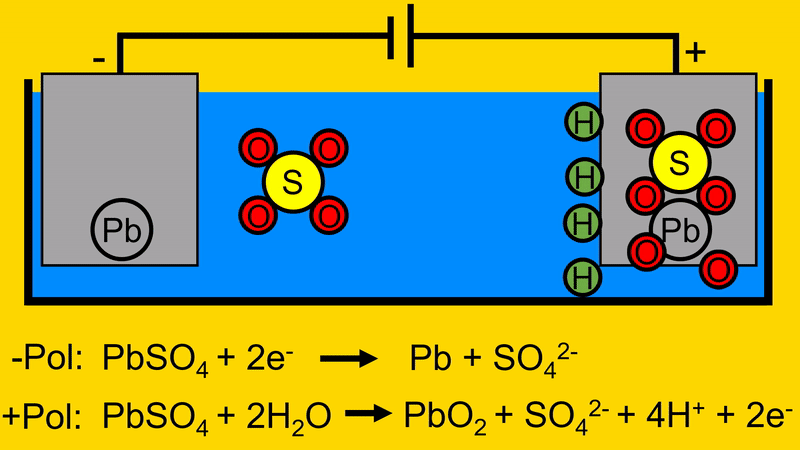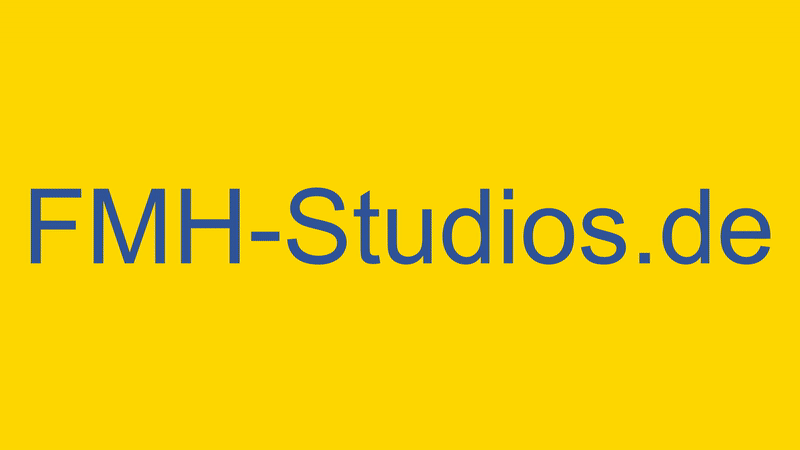
Durch diesen Vorgang trennt sich das Schwefeloxid von der positiven Elektrode.
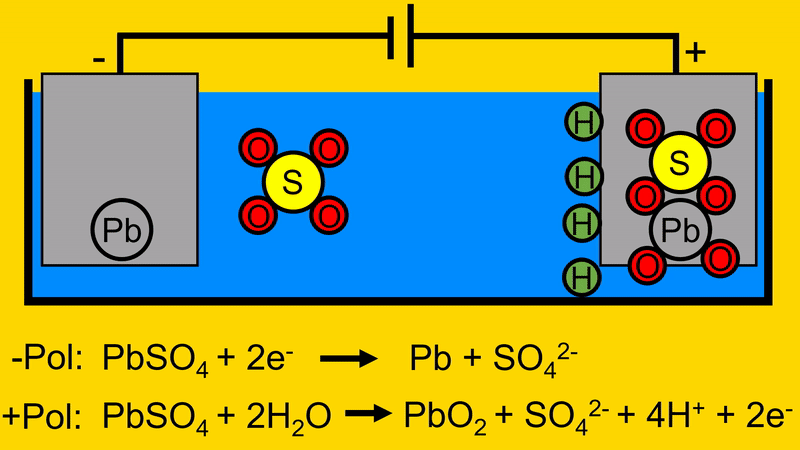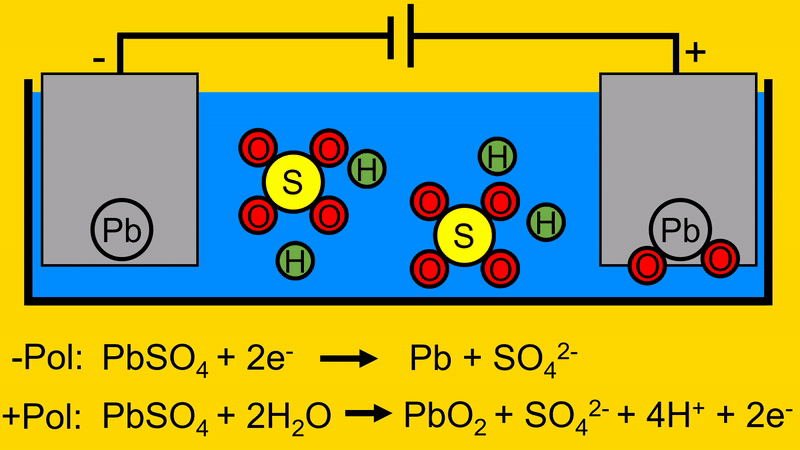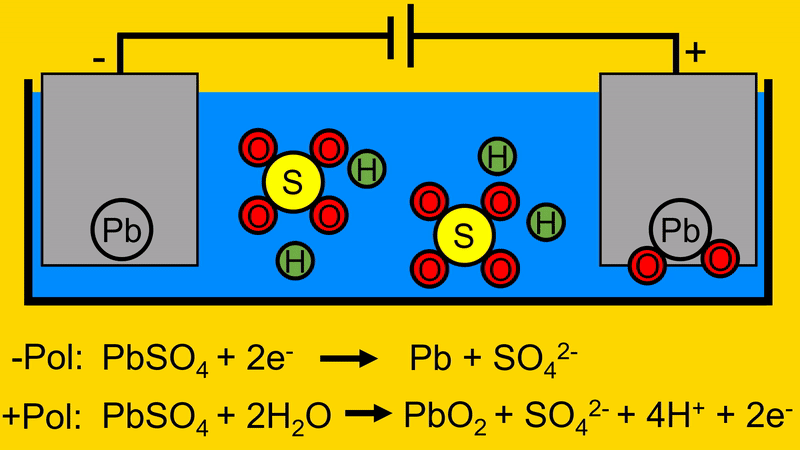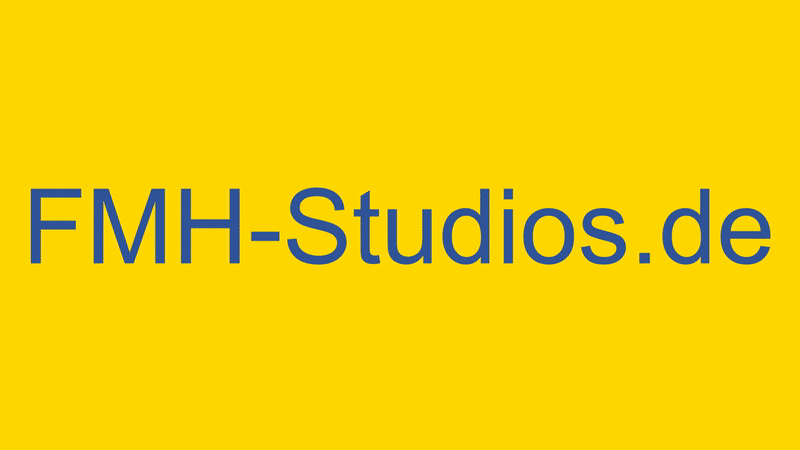
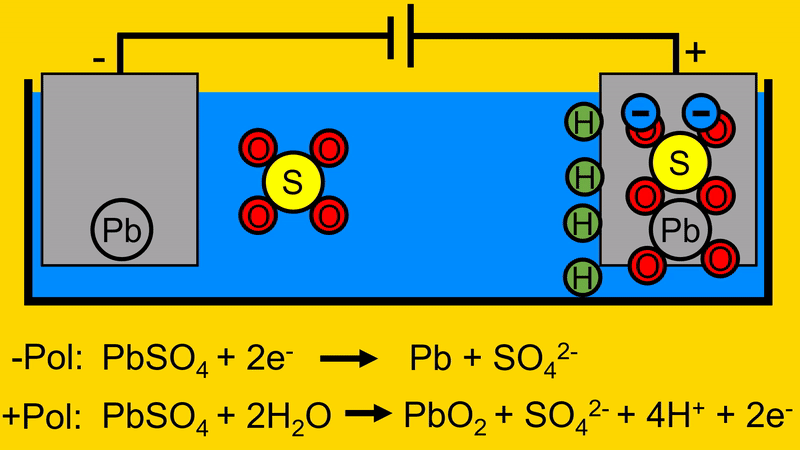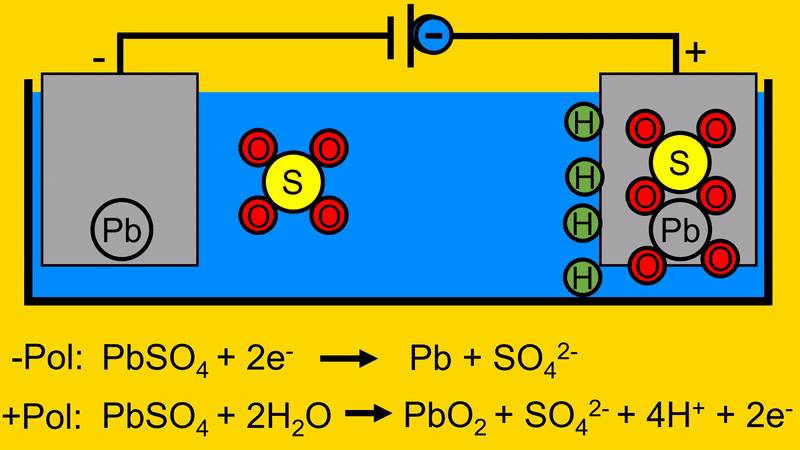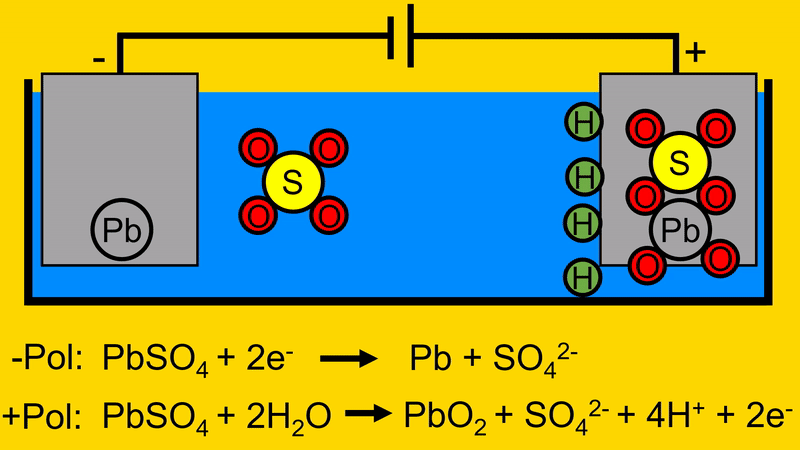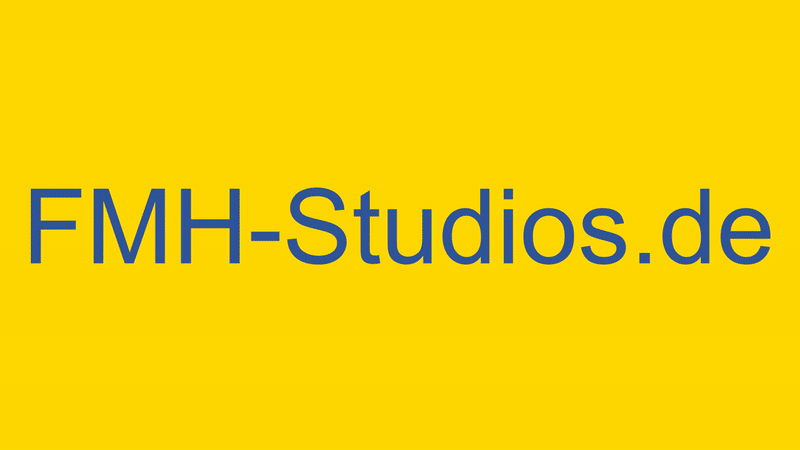
Durch das Entfernen des Schwefeloxids von der positiven Elektrode, werden Elektronen frei welche zur Spannungsquelle fließen.
Schritt für Schritt
→ Schritt 1:
Spannungsquelle wird angelegt
→ Schritt 2:
Elektronen fließen in die negative Elektrode.
→ Schritt 3:
Reaktion wird ausgelöst: -Pol: PbSO4 wird aufgespaltet. In Pb und SO4
→ Schritt 4:
Der Sauerstoff (O) aus dem Wasser (H2O) verbindet sich mit dem Blei-Schwefeloxid (PbSO4) aus der positiven Elektrode. H2 bleibt im Elektrolyt zurück.
→ Schritt 5:
Durch diesen Vorgang trennt sich das Schwefeloxid von der positiven Elektrode.
→ Schritt 6:
Hierdurch werden wiederum, an der positiven Elektrode, Elektronen frei gesetzt. Welche zur Quelle zurück fließen.
Zusammenfassung: